发布时间:2024-05-15 阅读量:
近日,我院徐建光副教授、王元银教授联合首都医科大学周建教授课题组,在《生物活性材料(Bioactive Materials)》(IF=18.9)发表题为《ETV2调节PHD2-HIF-1α轴控制代谢重编程促进血管化骨再生(ETV2 regulating PHD2-HIF-1α axis controls metabolism reprogramming promotes vascularized bone regeneration)》的学术论文。
该研究成果验证了转录因子ETS变体2(ETV2)在促进骨组织再生中的关键作用,通过调节能量代谢重编程和成骨与血管生成的协调,以及利用仿生纳米结构的羟基磷灰石/壳聚糖微球(HA/CS MS)增强干细胞功能,为治疗骨缺损提供了新的策略。我校校聘副教授李邦,硕士研究生杜浩然、于瑞为论文共同第一作者;徐建光、周建和王元银为本文的通讯作者,我校为第一作者单位。
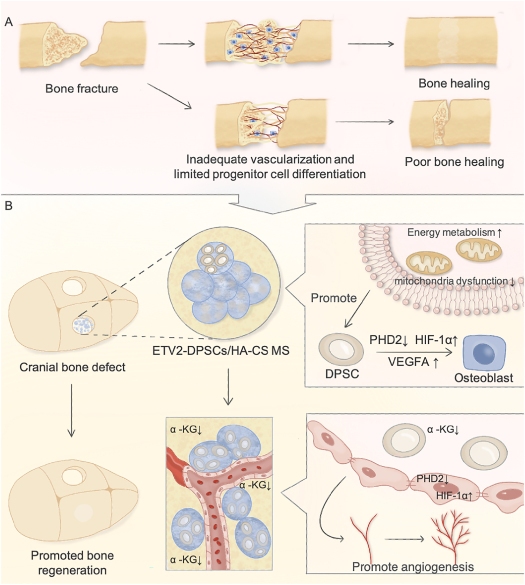
临界性骨缺损是颌面外科领域的常见疾病。由于骨祖细胞成骨诱导活性低和骨缺损处早期血管化不足,许多支架表现出有限的骨愈合能力。此外,能量代谢是多种生物过程的基础,成骨细胞相关的细胞增殖和分化是能量密集型过程。损害能量供应,MSC的增殖和分化受到阻碍,导致组织修复延迟并加剧原有损伤。因此,保证矿化骨和血管的早期同步发展,以及通过代谢重编程支持MSC分化是促进临界性骨缺损快速成功再生的关键。
该研究揭示了ETV2在调节细胞内HIF-1α稳态,影响成骨细胞成骨分化,重塑骨缺损区微环境,加速血管化骨再生作用。课题组首先发现在MSC的成骨谱系分化过程中伴随着ETV2的高表达;在人牙髓干细胞中,ETV2的瞬时激活能够维持细胞内HIF-1α稳态,并通过PHD2–HIF–1α-VEGFA轴促进成骨分化。此外,ETV2介导的DPSCs释放的α-KG减少,创造了一个缺氧信号稳态的血管生成生态位,促进内皮细胞迁移和血管结构的快速形成。
该研究团队利用羟基磷灰石/壳聚糖微球将ETV2-DPSC/MS复合物递送至大鼠颅骨缺损处,发现该复合物能有效加速骨再生。研究提出了一种新的治疗策略,通过调节缺氧信号稳态和能量代谢编程,实现快速血管生成和骨再生,对于治疗临界尺寸的骨缺损具有重要意义。
研究工作得到了国家自然科学基金、安徽省高等学校自然科学基金、北京市自然科学基金等项目的资助。
(正畸科 李邦)
原文链接:https://www.sciencedirect.com/science/article/pii/S2452199X24000598
时间:2024-05-14
来源:安徽医科大学
https://www.ahmu.edu.cn/2024/0514/c4325a157010/page.htm